Đừng lại gần tôi trong mọi trường hợp!
Tôi là phân tử nào?
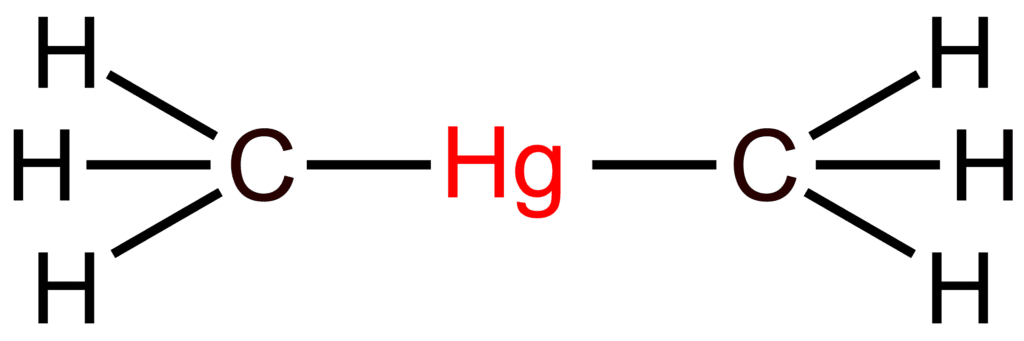
Thông tin nhanh về Dimetylmercury
| Số đăng ký CAS No. | 593-74-8 |
| Danh pháp SciFinder | Mercury, dimethyl- |
| Công thức thực nghiệm | C2H6Hg |
| Khối lượng phân tử | 230,66 g/mol |
| Trạng thái | Chất lỏng không màu |
| Điểm sôi | 93–94 °C |
| Độ hòa tan trong nước | Không hòa tan |
Đôi nét
Dimetylmercury (Me2Hg) là một trong những hóa chất độc hại nhất do con người tạo ra hoặc được tìm thấy trong tự nhiên. Nó đã được biết đến từ năm 1858, khi nhà hóa học/nhà côn trùng học người Anh George B. Buckton phân lập nó trong các thí nghiệm với các hợp chất metyl và etyl thủy ngân. Nó xuất hiện trở lại trong tài liệu vào năm 1899, khi nhà hóa học nổi tiếng người Pháp Marcellin Berthelot phát hiện ra rằng khi phóng điện Me2Hg hấp thụ khí nitơ.
Trong một phát hiện ban đầu về Me2Hg trong môi trường, các nhà nghiên cứu Thụy Điển S. Jensen và A. Jernelöv đã báo cáo vào năm 1969 rằng nó và sản phẩm phân hủy cation của nó, methylmercury1 (MeHg+), được tạo ra trong trầm tích đáy và cá thối trong vùng nước bị ô nhiễm thủy ngân. MeHg+ đã được sử dụng làm thuốc trừ sâu ở Thụy Điển cho đến năm 1966 và góp phần gây ô nhiễm cũng chẳng ích gì.
Kiến thức về sự phân bố của Me2Hg trong các đại dương đã bị hạn chế do thiếu các phương pháp đo lường. Trong nỗ lực giải quyết vấn đề này vào năm 2022, Robert P. Mason và các cộng tác viên tại Đại học Connecticut (Groton) và Đại học California, Santa Cruz, đã phát triển một máy phân tích tự động để đo độ phân giải cao của Me2Hg và thủy ngân dễ bay hơi khác các phân tử trong nước biển bề mặt.
Năm 1971, hai nhà khoa học Thụy Điển khác, Leif Bertilsson và Halina Y. Neujahr* tại Đại học Stockholm, đã chứng minh một cách khác rằng các hợp chất metyl thủy ngân được hình thành trong tự nhiên. Họ đã chỉ ra rằng methylcobalamin2, một dạng vitamin B12, phản ứng với ion thủy ngân(II) trong cơ thể người và động vật để tạo ra chất độc chết người.
Cái chết bi thảm năm 1997 của ngôi sao hóa học đang lên Karen Wetterhahn tại Đại học Dartmouth (Hanover, NH) đã khiến cho khả năng gây chết người của Me2Hg trở nên rõ ràng. Trong khi nghiên cứu về độc tính của kim loại nặng, Wetterhahn đã dính một lượng nhỏ Me2Hg vào găng tay cao su của mình, chất này sau đó được phát hiện là có thể thấm vào hợp chất. Bà ấy bắt đầu có các triệu chứng nhiễm độc, và chưa đầy một năm sau khi tiếp xúc, bà ấy đã chết. Vào năm 2022, kỷ niệm 25 năm ngày mất của bà, Sam Lemonick đã viết một bài tường thuật về cuộc đời và những đóng góp của Wetterhahn cho ngành hóa học.
Có một thời, Me2Hg được sử dụng làm chất metyl hóa trong tổng hợp hữu cơ; nhưng vì độc tính của nó, nó đã được thay thế bằng các thuốc thử an toàn hơn như dimethylzinc, trimethylaluminum và methylmagnesium halides (thuốc thử Grignard).
Để biết thêm thông tin về các tác động hóa học, độc tính và môi trường của Me2Hg, hãy xem trang thông tin ScienceDirect.
1. Số đăng ký CAS 22967-92-6.
2. Đăng ký CAS Số 13422-55-4.
Thông tin về nguy cơ Dimetylmercury
| Nhóm sự cố* | Mã GHS và tuyên bố nguy hiểm | |
|---|---|---|
| Chất lỏng dễ cháy, loại 2 | H225—Chất lỏng và hơi rất dễ cháy | |
| Độc tính cấp tính, đường miệng, loại 2 | H300—Tử vong nếu nuốt phải | |
| Độc cấp tính, qua da, loại 1 | H310—Tử vong khi tiếp xúc với da | |
| Độc tính cấp tính, hít phải, loại 2 | H330—Tử vong nếu hít phải | |
| Khả năng gây ung thư, loại 2 | H351—Nghi ngờ gây ung thư | |
| Độc tính cơ quan đích cụ thể, phơi nhiễm nhiều lần, loại 2 | H373—Có thể gây tổn thương các cơ quan khi phơi nhiễm kéo dài hoặc lặp đi lặp lại | |
| Nguy cơ thủy sinh (cấp tính) ngắn hạn, loại 1 | H400—Rất độc đối với thủy sinh vật | |
| Nguy cơ thủy sinh lâu dài (mãn tính), loại 1 | H410—Rất độc đối với thủy sinh vật với các tác động lâu dài |
*Hệ thống Hài hòa Toàn cầu (GHS) về Phân loại và Ghi nhãn Hóa chất. Giải thích về tượng hình
Tham khảo ACS.
