Thêm một axit vào nước và bạn có được tôi.
Tôi là phân tử nào?
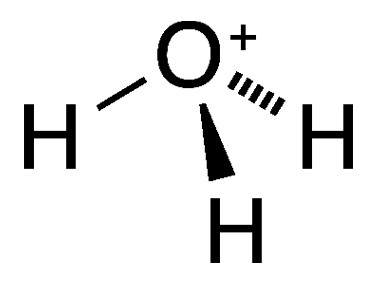
Sự thật nhanh về ion hydronium
| Số đăng ký CAS No | 13968-08-6 |
| Danh pháp SciFinder | Oxonium |
| Công thức thực nghiệm | H3O |
| Khối lượng phân tử | 19,02 g / mol |
| Trạng thái | Không thể bị cô lập |
| Khả năng hòa tan trong nước | Hòa tan hoàn toàn |
Tất cả các dung dịch nước có tính axit đều chứa nước proton, thường được gọi là ion hydronium (H3O+). Axit Brønsted giải phóng một hoặc nhiều proton của chúng (ion hydro), các proton này kết hợp với các phân tử nước. Các axit Lewis lấy một hoặc nhiều ion hydroxyl từ nước để giải phóng các ion hydro, và một lần nữa, tạo thành các ion hydronium.
Vì vậy, khi bạn thấy một phương trình hóa học nước có ký hiệu H+, hãy yên tâm rằng loại ion thực tế là H3O+.
Tại sao lại “oxonium” là tên ưu tiên cho ion hydronium? Đó là bởi vì hydronium là dạng ion oxonium đơn giản nhất, trong đó ba thực thể được gắn với một nguyên tử oxy, dẫn đến một điện tích dương thuần.
Khái niệm về ion hydronium đã được biết đến từ thế kỷ 19. Vào những năm 1880, nhà vật lý / hóa học người Thụy Điển Svante Arrhenius, làm việc với nhà hóa học người Đức Wilhelm Ostwald, đã định nghĩa axit là một chất phân ly trong nước để tạo thành các ion hydro, tạo ra ion hydronium trong nước. Axit proton được gọi là axit Arrhenius.
Arrhenius đã làm việc tại Viện Công nghệ Hoàng gia Thụy Điển (Stockholm) trong suốt sự nghiệp của mình. Sau đó trong sự nghiệp của mình, ông đã giúp thiết lập các giải thưởng Nobel. Ông đã giành được giải thưởng về hóa học vào năm 1903 cho các định nghĩa của mình về axit và bazơ.
Không chịu thua kém, Ostwald đã giành được giải Nobel Hóa học năm 1909 nhờ công trình nghiên cứu tốc độ phản ứng hóa học, sự cân bằng và xúc tác. Ông làm việc tại Viện Bách khoa Riga (Latvia) khi cộng tác với Arrhenius.
Ý tưởng của Arrhenius sau đó đã được Johannes Brønsted tại Đại học Copenhagen và Martin Lowry tại Đại học Cambridge (Anh) chắt lọc một cách độc lập. Axit proton ngày nay được gọi là axit Brønsted.
Tham khảo ACS.
