Tôi là một nguồn lithium siêu hòa tan.
Tôi là phân tử nào?
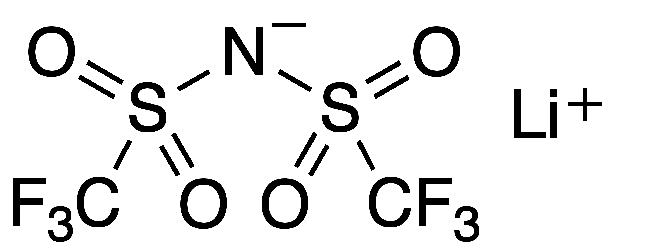
Sự thật nhanh về Lithium bis(trifluoromethane)sulfonimide
| Số đăng ký CAS No. | 90076-65-6 |
| Danh pháp Scifinder | Methanesulfonamide, 1,1,1-trifluoro-N-[(trifluoromethyl) sulfonyl]-, lithium salt (1:1) |
| Công thức thực nghiệm | C2F6LiNO4S2 |
| Khối lượng phân tử | 287,09 g / mol |
| Trạng thái | Bột trắng hút ẩm |
| Độ nóng chảy | 234–238 °C |
| Khả năng hòa tan trong nước | ≈6 kg / L |
Đôi nét
Lithium bis(trifluoromethane)sulfonimide (LiTFSI) là một loại muối hữu cơ ưa nước có nhiều ứng dụng trong hệ thống điện và điện tử. Anion sulfonimide bis(trifluoromethane) của nó, thường được gọi là bistriflimide, có đặc tính hữu ích là phối hợp yếu với các cation.
Đặc tính quan trọng khác của LiTFSI là khả năng hòa tan cực cao trong nước: 21 molal hoặc ≈6 kg / L dung dịch. Do tính hòa tan của nó, nó đã được khám phá như một chất điện phân cho pin lithium-ion, pin mặt trời và các ứng dụng tương tự ít nhất là từ cuối những năm 1980. LiTFSI là một vật liệu an toàn hơn muối được sử dụng trước đây, lithium hexafluorophosphate (LiPF6).
Trong một bài báo trên Nature năm 2021, André D. Taylor tại Đại học New York (Thành phố New York) và Đại học Yale (New Haven, CT) cùng 18 đồng nghiệp ở đó và tại các tổ chức khác ở Hoa Kỳ và Hàn Quốc đã báo cáo một sự sàng lọc trong sử dụng LiTFSI trong pin mặt trời.
Tế bào quang điện làm bằng perovskite hấp thụ ánh sáng rẻ tiền có hiệu suất chuyển đổi năng lượng cao đã được phát triển trong vài năm qua. Để cải thiện khả năng vận chuyển điện tích của tế bào, chúng được pha tạp chất với sự kết hợp của LiTFSI và chất bán dẫn được gọi là Spiro-OMeTAD1; nhưng quá trình này diễn ra cực kỳ chậm.
Taylor và các nhà nghiên cứu đồng nghiệp của ông đã giải quyết vấn đề này bằng cách sủi bọt khí carbon dioxide thành dung dịch spiro-OMeTAD và LiTFSI trong khi chiếu xạ hỗn hợp bằng tia cực tím. Sau đó, họ đặt một bộ phim làm từ dung dịch này lên chất hấp thụ ánh sáng perovskite. Quá trình này có thể được hoàn thành trong ≈1 phút, so với quy trình sử dụng doping cũ hơn, kéo dài hàng giờ đồng hồ.
Các tác giả cho biết, “Lớp xen kẽ được xử lý CO2 thể hiện độ dẫn điện cao hơn xấp xỉ 100 lần so với màng nguyên sinh [chưa được xử lý] đồng thời tạo ra các tế bào năng lượng mặt trời ổn định, hiệu suất cao mà không cần bất kỳ xử lý nào sau xử lý”. Họ cũng báo cáo rằng phương pháp của họ rất hữu ích để pha tạp các polymer liên hợp π.
1. 2,2 ′, 7,7′-Tetrakis [N , N -di (4-metoxyphenyl) amino] -9,9-spirobifluorene, CAS Reg. Số 207739-72-8.
Thông tin về mối nguy hiểm của Lithium bis(trifluoromethane)sulfonimide *
| Nhóm sự cố** | Mã GHS và tuyên bố nguy cơ | |
|---|---|---|
| Độc tính cấp, đường uống, loại 3 | H301 — Độc nếu nuốt phải | |
| Độc tính cấp, qua da, loại 3 | H311 — Độc khi tiếp xúc với da | |
| Ăn mòn / kích ứng da, loại 1B | H314 — Gây bỏng da nghiêm trọng và tổn thương mắt | |
| Tổn thương mắt nghiêm trọng / kích ứng mắt, loại 1 | H318 — Gây tổn thương mắt nghiêm trọng | |
| Độc tính đối với cơ quan đích cụ thể (hệ thần kinh), phơi nhiễm nhiều lần, qua đường miệng, loại 2 | H373 — Có thể gây tổn thương hệ thần kinh khi tiếp xúc lâu dài hoặc lặp lại nếu nuốt phải | |
| Mối nguy thủy sinh ngắn hạn (cấp tính), loại 3 | H402 — Có hại cho đời sống thủy sinh | |
| Mối nguy thủy sinh lâu dài (mãn tính), loại 3 | H412 — Có hại cho đời sống thủy sinh với những ảnh hưởng lâu dài |
* Biên soạn các phiếu dữ liệu an toàn đã chọn.
** Hệ thống hài hòa toàn cầu (GHS) về phân loại và ghi nhãn hóa chất. Giải thích từ tượng hình.
Tham khảo ACS.
