Giải thưởng Nobel hóa học 2019 được trao cho 3 nhà khoa học từ Anh, Mỹ và Nhật cho sự công trình phát triển pin lithium-ion góp phần “sạc lại thế giới”.
Chủ đề này nghe có vẻ rất thú vị, nhưng có bao nhiêu bạn đang đọc bài viết này hiểu rõ về pin lithium-ion?
Vì thế trong bài viết lần này, blog sẽ giúp các bạn hiểu rõ hơn về loại pin này cũng như những điều thú vị về hóa học đằng sau.
Trước khi đi vào nội dung chính của bài, chúng ta sẽ tìm hiểu một vài thông tin cơ bản trước đã. Các bạn đã sẵn sàng chưa nào? Hãy nhâm nhi một tách cà phê và cùng tận thưởng bài viết nhé!
Pin là gì?
Pin là một bộ năng lượng hóa học khép kín, có thể tạo ra một lượng năng lượng điện hạn chế ở bất cứ nơi nào cần thiết.
Không giống như điện thông thường, chạy vào nhà bạn thông qua các dây điện bắt đầu từ nhà máy điện, pin từ từ chuyển đổi các hóa chất được đóng gói bên trong thành năng lượng điện, thường được giải phóng trong khoảng thời gian vài ngày, vài tuần, vài tháng hoặc thậm chí nhiều năm.
Ý tưởng cơ bản về năng lượng di động không có gì mới; con người luôn có cách tạo ra năng lượng khi di chuyển.
Ngay cả con người thời tiền sử cũng biết cách đốt củi để tạo ra lửa, đó là một cách sản xuất năng lượng (dưới dạng nhiệt) hoặc từ hóa chất (đốt cháy giải phóng năng lượng bằng cách sử dụng phản ứng hóa học gọi là đốt cháy).
Vào thời Cách mạng Công nghiệp (vào thế kỷ 18 và 19), chúng ta đã thành thạo nghệ thuật đốt các cục than để tạo ra năng lượng, vì vậy đã thúc đẩy mọi thứ như đầu máy hơi nước.
Nhưng có thể mất một giờ để thu thập đủ gỗ để nấu một bữa ăn, và nồi hơi của đầu máy thường mất vài giờ để đủ nóng để tạo hơi nước.
Trong khi đó pin thì ngược lại, cung cấp cho chúng ta năng lượng tức thời, di động. Bạn chỉ cần vặn chìa khóa trong xe điện của bạn và nó bắt đầu cuộc sống trong vài giây!

Các bộ phận chính của pin là gì?
Đơn vị năng lượng cơ bản bên trong pin được gọi là một tế bào (hay cell) và nó bao gồm ba bit (hay đơn vị) chính.
Có hai điện cực (thiết bị đầu cuối điện) và một hóa chất gọi là chất điện phân ở giữa chúng.
Để thuận tiện và an toàn cho chúng ta, những thứ này thường được đóng gói bên trong vỏ ngoài bằng kim loại hoặc nhựa.
Có hai thiết bị đầu cuối điện tiện dụng hơn, được đánh dấu bằng một dấu cộng (dương) và một dấu âm (âm), ở bên ngoài được kết nối với các điện cực bên trong.
Sự khác biệt giữa pin và tế bào chỉ đơn giản là pin bao gồm hai hoặc nhiều tế bào được nối với nhau để năng lượng của chúng cộng lại với nhau.
Khi bạn kết nối hai điện cực của pin với một mạch điện (ví dụ: khi bạn đặt một điện cực vào đèn pin), chất điện phân bắt đầu rì rầm với hoạt động. Dần dần, các hóa chất bên trong nó được chuyển đổi thành các chất khác.
Các ion (nguyên tử có quá ít hoặc quá nhiều electron) được hình thành từ các vật liệu trong các điện cực và tham gia vào các phản ứng hóa học với chất điện phân.
Đồng thời, các electron di chuyển từ cực này sang cực kia qua mạch ngoài, cung cấp năng lượng cho bất cứ thứ gì pin được kết nối.
Quá trình này tiếp tục cho đến khi chất điện phân được biến đổi hoàn toàn. Tại thời điểm đó, các ion ngừng di chuyển qua chất điện phân, các electron ngừng chảy qua mạch và pin bị xẹp.
Sơ lược về lịch sử của pin
- 250 BC–AD 224: Một số nhà sử học cho rằng pin đầu tiên được phát minh vào khoảng thời gian này, dựa trên khám phá khảo cổ học về các mảnh sắt và đồng (giống như các điện cực) và một bình đất sét gần Baghdad vào những năm 1930. Mặc dù phát hiện này vẫn thường được gọi là “pin Baghdad” hoặc “pin Parthian” (tên được đặt sau nơi nó được phát hiện và thời kỳ lịch sử mà nó có từ đó), các nhà sử học khác nghi ngờ liệu trên thực tế nó có tạo ra dòng điện hay không có chức năng như một cục pin.
- 1744: Ewald Georg von Kleist (1700-1748) phát minh ra chiếc bình Leyden, một hộp đựng bằng thủy tinh có lá kim loại ở cả mặt trong và mặt ngoài sẽ tích điện. Mặc dù nó thực sự là một tụ điện (một thiết bị lưu trữ tĩnh điện), nhưng nó phục vụ cùng một mục đích như một loại pin hiện đại: đó là một cửa hàng năng lượng điện cầm tay. (Rất nhiều thí nghiệm ban đầu về điện đã sử dụng bình Leyden làm nguồn năng lượng của chúng, nơi chúng ta sẽ sử dụng pin ngày nay.)
- 1749: Chính trị gia và nhà phát minh người Mỹ Benjamin Franklin (1706-1790) lần đầu tiên sử dụng thuật ngữ “pin” để chỉ một số tụ điện được kết nối với nhau.
- 1800: Nhà vật lý người Ý Alessandro Volta (1745-1827) phát minh ra cọc Voltaic, pin thực tế đầu tiên. Ông thực hiện bằng cách xếp chồng các đĩa kẽm và bạc, xen kẽ, ngăn cách bằng bìa cứng và ngâm trong nước mặn.
- Những năm 1800: Nhà hóa học người Anh Humphry Davy (1778-1829) sử dụng cọc Voltaic và điện phân để cô lập một số nguyên tố hóa học, bao gồm natri và kali.
- 1836: Nhà hóa học người Anh John Daniell (1790-1845) phát minh ra tế bào Daniell, một loại pin đáng tin cậy hơn.
- Những năm 1840: Một linh mục người Ailen tên là Cha Nicholas Joseph Callan (1799-1886) phát triển dây điện lên tới 577 tế bào riêng lẻ để chế tạo pin lớn nhất thế giới tại thời điểm đó.
- 1859: Bác sĩ người Pháp Gaston Planté ( 1834-1889) phát triển loại pin axit chì có thể sạc lại đầu tiên trên thế giới.
- 1868: Một người Pháp khác, Georges Leclanché (1839-1882), phát triển pin kẽm-carbon hiện đại.
- 1881: Kỹ sư người Pháp Camille Alphonse Faure (1840-1898) thiết kế lại pin axit-chì, cho phép lần đầu tiên nó được sản xuất trên quy mô lớn.
- Những năm 1880: Pin khô được phát triển độc lập bởi một số nhà phát minh khác nhau, bao gồm cả người Đan Mạch Frederik Louis Wilhelm Hellesen (1836-1892) và Đức Carl Gassner (1839-1882).
- 1888: Nhiều thập kỷ trước khi khái niệm năng lượng tái tạo trở nên phổ biến, nhà tiên phong về điện của Mỹ Charles F. Brush (1849-1929) chế tạo một tuabin gió có khả năng sạc một lượng lớn pin để cung cấp năng lượng cho ngôi nhà của mình.
- 1949: Kỹ sư hóa học người Canada Lewis Urry (1927-2004) phát minh ra pin kiềm và pin lithium cho công ty Pin Eveready.
- 1971: Wilson Greatbatch (1919-2011), một kỹ sư người Mỹ, người tiên phong sử dụng pin lithium-iodide có tuổi thọ cao, không bị ăn mòn để sử dụng trong máy tạo nhịp tim cấy ghép.
- Những năm 1970: Khi làm việc tại Đại học Oxford ở Anh, nhà hóa học người Mỹ gốc Đức John B. Goodenough (1922-) và các đồng nghiệp của ông đã tìm ra khoa học đằng sau pin lithium-ion. Pin thương mại đầu tiên sử dụng công nghệ được Sony phát triển vào những năm 1990.
- 2017: John B. Goodenough cấp bằng sáng chế pin dựa trên thủy tinh lithium hoặc natri có thể thay thế công nghệ lithium-ion trong tương lai.
Tại sao pin cần hai vật liệu khác nhau?
Điều quan trọng cần lưu ý là các điện cực trong pin luôn được chế tạo từ hai vật liệu không giống nhau (vì vậy không bao giờ cả hai từ cùng một kim loại), mà rõ ràng phải là chất dẫn điện.
Đây là chìa khóa để làm thế nào và tại sao pin hoạt động: một trong những vật liệu “thích” từ bỏ điện tử, cái còn lại thích nhận chúng.
Nếu cả hai điện cực được làm từ cùng một vật liệu, điều đó sẽ không xảy ra và không có dòng điện nào chảy qua cả.
Để hiểu điều này, chúng ta cần đi sâu vào lịch sử điện đến năm 1792, khi nhà khoa học người Ý Luigi Galvani nhận thấy ông ta có thể tạo ra điện với một chút trợ giúp từ chân ếch.
Điển hình, Galvani đã nhét một vài kim loại khác nhau vào chân của một con ếch đã chết và tạo ra một dòng điện, mà ông tin rằng nó được tạo ra bởi con ếch giải phóng “điện động vật” của nó.
Trên thực tế, khi người đồng hương Alessandro Volta sớm nhận ra điều quan trọng là Galvani đã sử dụng hai kim loại khác nhau.
Do đó, cơ thể của con ếch đã hoạt động như chất điện phân của pin được làm bằng hai điện cực kim loại khác nhau mắc kẹt trong đó.
Sống hay chết, không có gì đặc biệt về con ếch; một lọ thủy tinh chứa đầy các hóa chất phù hợp hoặc thậm chí một lát chanh cũng sẽ hoạt động tốt.
Điều gì đặc biệt về các điện cực? Các nguyên tố hóa học khác nhau về khả năng kéo các electron về phía chúng hoặc đưa chúng lên các nguyên tố khác kéo chúng nhiều hơn.
Chúng ta gọi xu hướng này là độ âm điện. Dán hai kim loại khác nhau vào một chất điện phân, sau đó kết nối chúng thông qua một mạch ngoài và bạn sẽ có một cuộc giằng co đang diễn ra giữa chúng.
Một trong những kim loại thắng và kéo các electron từ bên kia, thông qua mạch ngoài cùng và dòng điện tử từ kim loại này sang kim loại khác là cách pin cung cấp năng lượng cho mạch.
Nếu hai cực của pin được làm từ cùng một vật liệu, sẽ không có dòng điện tử ròng và sẽ không có năng lượng nào được tạo ra.
Dù sao đó cũng là lý thuyết. Bây giờ hãy nhìn vào nó trong thực tế nhé!
Bây giờ trở lại pin của chúng ta. Các điện cực dương và âm được phân tách bằng chất điện phân hóa học.
Nó có thể là một chất lỏng, nhưng trong một pin thông thường, nó có nhiều khả năng là một loại bột khô.
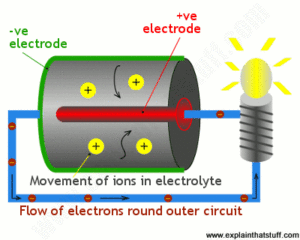
Khi bạn kết nối pin với đèn và bật, các phản ứng hóa học bắt đầu xảy ra.
Một trong những phản ứng tạo ra các ion dương (hiển thị ở đây là các đốm màu vàng lớn) và các electron (các đốm màu nâu nhỏ hơn) ở điện cực âm.
Các ion dương chảy vào chất điện phân, trong khi các electron (các đốm màu nâu nhỏ hơn) chảy xung quanh mạch ngoài (đường màu xanh) đến điện cực dương và làm cho đèn sáng lên trên đường đi.
Có một phản ứng hóa học riêng biệt xảy ra ở điện cực dương, trong đó các electron tới tái hợp với các ion được lấy ra khỏi chất điện phân, do đó hoàn thành mạch.
Các electron và ion chảy vì các phản ứng hóa học xảy ra bên trong pin, thường là hai trong số chúng xảy ra đồng thời. Các phản ứng chính xác phụ thuộc vào vật liệu mà từ đó các điện cực và chất điện phân được tạo ra.
Bất kể phản ứng hóa học diễn ra, nguyên tắc chung của các electron đi xung quanh mạch ngoài và các ion phản ứng với chất điện phân (di chuyển vào nó hoặc ra khỏi nó), áp dụng cho tất cả các pin.
Khi pin tạo ra năng lượng, các hóa chất bên trong nó dần dần được chuyển đổi thành các hóa chất khác nhau.
Khả năng tạo ra sự suy giảm năng lượng của chúng, điện áp của pin giảm dần và pin cuối cùng sẽ bị xẹp.
Nói cách khác, nếu pin không thể tạo ra các ion dương vì các hóa chất bên trong nó đã cạn kiệt, nó cũng không thể tạo ra các electron cho mạch ngoài.
Bây giờ bạn có thể nghĩ: “Đợi đã, điều này không có ý nghĩa gì cả! Tại sao các electron không cắt ngắn và nhảy thẳng từ điện cực âm qua chất điện phân đến điện cực dương?
Về mặt hóa học của chất điện phân, các electron không thể chảy qua nó theo cách đơn giản này.
Thực tế, đối với các điện tử có liên quan, chất điện phân gần như là một chất cách điện: một rào cản mà chúng không thể vượt qua điện cực thực sự bằng cách chảy qua mạch ngoài.
Sự cố với pin thông thường
Đến đây thì bạn đã biết pin về cơ bản là một thí nghiệm hóa học xảy ra trong một hộp kim loại nhỏ.
Kết nối hai đầu pin với một cái gì đó giống như đèn pin và các phản ứng hóa học bắt đầu: các hóa chất bên trong pin chậm nhưng tách ra một cách có hệ thống và liên kết với nhau để tạo ra các hóa chất khác, tạo ra một dòng các hạt tích điện dương gọi là ion và electron tích điện âm.
Các ion di chuyển qua pin; các electron đi qua mạch mà pin được kết nối, cung cấp năng lượng điện làm sáng đèn pin.
Vấn đề duy nhất là, phản ứng hóa học này chỉ có thể xảy ra một lần và chỉ theo một hướng: đó là lý do tại sao pin thông thường thường không thể sạc lại được.Vì thế mà pin pin sạc bằng phản ứng thuận nghịch ra đời.
Các hóa chất khác nhau được sử dụng trong pin sạc và chúng tách ra thông qua các phản ứng hoàn toàn khác nhau.
Sự khác biệt lớn là các phản ứng hóa học trong pin sạc có thể đảo ngược: khi pin xả hết các phản ứng đi một chiều và pin hết điện; khi pin đang sạc, các phản ứng đi theo hướng ngược lại và pin sẽ hấp thụ năng lượng.
Những phản ứng hóa học này có thể xảy ra hàng trăm lần ở cả hai hướng, do đó, pin sạc thường sẽ cung cấp cho bạn mọi thứ từ hai hoặc ba đến 10 năm tuổi thọ (tùy thuộc vào tần suất bạn sử dụng và mức độ chăm sóc của bạn).
Pin lithium-ion hoạt động như thế nào?
Giống như bất kỳ loại pin nào khác, pin lithium-ion có thể sạc lại được tạo thành từ một hoặc nhiều ngăn tạo ra năng lượng gọi là tế bào.
Mỗi tế bào về cơ bản có ba thành phần: một điện cực dương (được kết nối với cực dương của pin), một điện cực âm (được kết nối với cực âm của pin) và một hóa chất gọi là chất điện phân ở giữa chúng.
Điện cực dương thường được chế tạo từ một hợp chất hóa học gọi là oxit lithium-coban (LiCoO2) hoặc, trong pin mới hơn, từ lithium sắt phosphate (LiFePO4).
Điện cực âm thường được làm từ carbon (than chì) và chất điện phân thay đổi từ loại pin này sang loại pin khác, nhưng không quá quan trọng trong việc tìm hiểu ý tưởng cơ bản về cách thức hoạt động của pin.
Tất cả các pin lithium-ion hoạt động theo cùng một cách. Khi pin được sạc đầy, oxit lithium-coban, điện cực dương sẽ nhường một số ion lithium của nó, di chuyển qua chất điện phân đến điện cực than chì, âm và vẫn ở đó.
Pin lấy và lưu trữ năng lượng trong quá trình này. Khi pin được xả, các ion lithium di chuyển trở lại qua chất điện phân đến điện cực dương, tạo ra năng lượng cung cấp năng lượng cho pin.
Trong cả hai trường hợp, các electron chảy theo hướng ngược lại với các ion xung quanh mạch ngoài.
Các electron không chảy qua chất điện phân: đó thực sự là một rào cản cách điện, cho đến khi có liên quan đến các điện tử.
Sự chuyển động của các ion (thông qua chất điện phân) và các electron (xung quanh mạch ngoài, theo hướng ngược lại) là các quá trình liên kết với nhau, và nếu một trong hai dừng lại thì điều đó cũng xảy ra.
Nếu các ion ngừng di chuyển qua chất điện phân vì pin hết hoàn toàn, các electron không thể di chuyển qua mạch ngoài hoặc vì vậy bạn sẽ mất điện.
Tương tự, nếu bạn tắt bất cứ thứ gì pin đang cung cấp năng lượng, dòng điện tử sẽ dừng lại và dòng ion cũng vậy. Pin về cơ bản dừng xả ở tốc độ cao (nhưng nó vẫn tiếp tục xả, ở tốc độ rất chậm, ngay cả khi thiết bị bị ngắt kết nối).
Không giống như pin đơn giản hơn, pin lithium-ion được tích hợp bộ điều khiển điện tử điều chỉnh cách chúng sạc và xả.
Chúng ngăn chặn việc sạc quá mức và quá nóng có thể khiến pin lithium-ion phát nổ trong một số trường hợp.
Vậy chúng sạc và xả như thế nào?
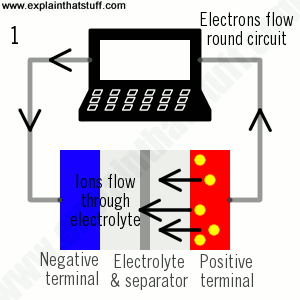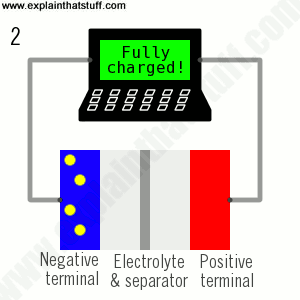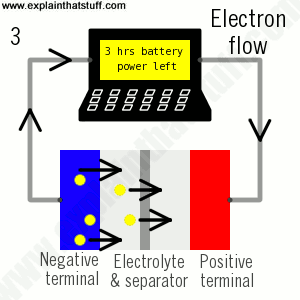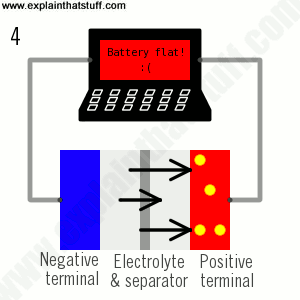
Pin lithium-ion là tất cả về sự chuyển động của các ion lithium: các ion di chuyển một chiều khi pin sạc (khi nó hấp thụ năng lượng); chúng di chuyển ngược lại khi pin hết (khi nó cung cấp năng lượng):
- Trong quá trình sạc, các ion lithium (vòng tròn màu vàng) chảy từ điện cực dương (màu đỏ) sang điện cực âm (màu xanh) qua chất điện phân (màu xám). Các electron cũng chảy từ điện cực dương sang điện cực âm, nhưng đi theo con đường dài hơn xung quanh mạch ngoài. Các electron và ion kết hợp ở điện cực âm và lắng đọng lithium ở đó.
- Khi không còn các ion sẽ chảy, pin được sạc đầy và sẵn sàng để sử dụng.
- Trong quá trình phóng điện, các ion chảy ngược qua chất điện phân từ điện cực âm sang điện cực dương. Electron chảy từ điện cực âm sang điện cực dương qua mạch ngoài, cung cấp năng lượng cho máy tính xách tay của bạn. Khi các ion và electron kết hợp ở điện cực dương, lithium được lắng đọng ở đó.
- Khi tất cả các ion đã di chuyển trở lại, pin đã được xả hết và cần sạc lại.
Các ion lithium được lưu trữ như thế nào?
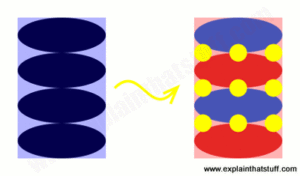
Hoạt hình thứ hai này cho thấy những gì đang diễn ra trong pin chi tiết hơn một chút.
Một lần nữa, điện cực than chì âm tính (màu xanh) được hiển thị ở bên trái, điện cực coban-oxit dương tính (màu đỏ) ở bên phải và các ion lithium được thể hiện bằng các vòng tròn màu vàng.
Khi pin được sạc đầy, tất cả các ion lithium được lưu trữ giữa các lớp graphene (các tấm carbon dày một nguyên tử) trong điện cực than chì (tất cả chúng đã di chuyển sang bên trái).
Ở trạng thái sạc điện này, pin thực sự là một bánh sandwich nhiều lớp: các lớp graphene xen kẽ với các lớp ion lithium. Khi pin xả, các ion di chuyển từ điện cực than chì sang điện cực coban-oxit (từ trái sang phải).
Khi nó được phóng điện hoàn toàn, tất cả các ion lithium đã chuyển sang điện cực oxit coban ở bên phải. Một lần nữa, các ion lithium ngồi thành lớp, ở giữa các lớp ion coban (màu đỏ) và ion oxit (màu xanh).
Khi pin sạc và xả, các ion lithium chuyển qua lại từ điện cực này sang điện cực khác.
Ưu và nhược điểm của pin lithium-ion
- Ưu điểm
Nói chung, pin lithium ion đáng tin cậy hơn các công nghệ cũ như niken-cadmium (NiCd, gọi tắt là nicad) và không gặp phải vấn đề gọi là “hiệu ứng bộ nhớ” (trong đó pin nicad dường như khó sạc hơn trừ khi chúng được phóng điện đầy đủ trước).
Vì pin lithium-ion không chứa cadmium (một kim loại nặng, độc hại), nên về mặt lý thuyết, chúng cũng tốt hơn cho môi trường.
Mặc dù chúng ta thường bỏ bất kỳ loại pin nào (đầy kim loại, nhựa và các loại hóa chất khác) vào bãi rác không bao giờ là một điều tốt.
So với pin sạc nặng (như pin chì-axit dùng để khởi động ô tô), pin lithium-ion tương đối nhẹ đối với lượng năng lượng mà chúng lưu trữ.
- Nhược điểm
Nếu chúng ta quan tâm đến những nhược điểm của pin lithium-ion, điều quan trọng là phải ghi nhớ những gì chúng ta đang so sánh với chúng.
Pin này là một nguồn năng lượng cho ô tô, chúng ta thực sự cần phải so sánh chúng không phải với các loại pin khác mà với xăng.
Mặc dù đã có những tiến bộ đáng kể trong những năm qua, pin sạc vẫn chỉ lưu trữ một phần năng lượng như khí đốt thông thường.
Nói một cách khoa học hơn, chúng có mật độ năng lượng thấp hơn nhiều (chúng lưu trữ ít năng lượng hơn trên mỗi đơn vị trọng lượng).
Điều đó cũng giải thích lý do tại sao bạn hoàn toàn có thể “sạc lại” (tiếp nhiên liệu) cho một chiếc ô tô chạy bằng khí trong vài phút, trong khi nó thường sẽ khiến bạn mất hàng giờ để sạc pin trong xe điện.
Sau đó, một lần nữa, bạn phải nhớ rằng những nhược điểm này được cân bằng bởi những lợi thế khác, chẳng hạn như tiết kiệm nhiên liệu hơn của ô tô điện và ít ô nhiễm không khí tương đối (không thải khí thải / khí thải từ chính chiếc xe).
Bỏ xe sang một bên và xem xét pin lithium-ion nói chung, vấn đề là gì?
Vấn đề lớn nhất là sự an toàn: Pin Li-ion sẽ bốc cháy nếu chúng bị sạc quá mức hoặc nếu sự cố bên trong gây ra đoản mạch; trong cả hai trường hợp, pin nóng lên trong cái gọi là “chạy trốn nhiệt”, cuối cùng bắt lửa hoặc phát nổ.
Vấn đề đó được giải quyết với bộ ngắt mạch tích hợp, được gọi là thiết bị ngắt dòng hoặc CID, sẽ giết chết dòng sạc khi điện áp đạt đến mức tối đa, nếu pin quá nóng hoặc áp suất bên trong của chúng tăng quá cao.
Nhưng vẫn còn những lo ngại vì thế năm 2016, Tổ chức Hàng không Dân dụng Quốc tế đã chính thức cấm các lô hàng pin lithium-ion trên máy bay chở khách vì mối nguy hiểm tiềm tàng.
Một vài sự cố đã được đưa ra mức độ phổ biến của công nghệ (bạn sẽ tìm thấy pin lithium-ion trong mọi điện thoại di động, máy tính xách tay, máy tính bảng hiện đại và hầu hết các thiết bị sạc khác).
Và một lần nữa, điều quan trọng là phải ghi nhớ những rủi ro của các giải pháp thay thế: vâng, pin lithium-ion trong ô tô điện có thể bắt lửa, nhưng ô tô chạy bằng xăng bắt lửa thường xuyên hơn … và gây ra vụ nổ thực sự!
Các loại pin khác cũng có thể bắt lửa và phát nổ nếu chúng quá nóng, do đó, lửa không phải là vấn đề duy nhất đối với công nghệ lithium-ion.
Giải pháp là gì? Một lựa chọn đầy hứa hẹn, hiện đang được tiên phong bởi một công ty có tên là Ionic Material, là sử dụng các polymer chống cháy (nhựa rắn) thay cho các chất điện phân lỏng dễ cháy thường được sử dụng trong pin lithium-ion.
Một lựa chọn khác, được ưa chuộng bởi John Goodenough, nhà hóa học đứng sau pin lithium-ion, là sử dụng thủy tinh “pha tạp” (được xử lý để làm cho nó dẫn điện) cho chất điện phân thay thế.
Thời gian sẽ cho biết liệu một trong những tùy chọn này có thể là một trong những tùy chọn khác hay không, một thứ gì đó hoàn toàn khác sẽ vượt qua pin lithium-ion từ vị trí của chúng như là công nghệ sạc yêu thích của thế giới.
Trên đây là những điều thú vị về pin cũng như pin lithium-ion. Hi vọng sẽ giúp ích cho các bạn phần nào trong tương lai.
Lần sau nếu có ai hỏi về chúng thì hãy nhớ đến hóa học đằng sau chúng nhé!
Theo Explainthatstuff và tổng hợp.
