Bài viết này được dịch và biên tập lại từ bài viết: “The tangled history of mRNA vaccines” của tác giả Elie Dolgin trên tạp chí Nature để giúp cho các bạn có cái nhìn rõ hơn về lịch sử ra đời và các câu chuyện thú vị xoay quanh vắc-xin mRNA.
Bài viết khá dài gồm 11 tiêu đề, vì thế tôi đã bổ sung phần mục lục bên dưới để các bạn tiện theo dõi. Nếu bạn giỏi Anh ngữ thì vào bài viết gốc xem để ủng hộ tác giả. Xin cảm ơn!
Hàng trăm nhà khoa học đã nghiên cứu vắc-xin mRNA trong nhiều thập kỷ trước khi đại dịch coronavirus mang lại một bước đột phá.
Theo Nature.
Bước đi đầu tiên
Cuối năm 1987, Robert Malone thực hiện một thí nghiệm mang tính bước ngoặt. Ông trộn các sợi mRNA với các giọt chất béo, để tạo ra một loại bể phân tử.
Các tế bào của con người được tắm trong “súp” di truyền này đã hấp thụ mRNA và bắt đầu sản xuất các protein từ nó.
Nhận thấy rằng khám phá này có thể có tiềm năng sâu rộng trong y học, Malone, một nghiên cứu sinh tại Viện Nghiên cứu Sinh học Salk ở La Jolla, California, sau đó đã ghi lại một số ghi chú, mà ông ấy đã ký tên và ghi ngày tháng.
Ông đã viết vào ngày 11 tháng 1 năm 1988 nếu tế bào có thể tạo ra protein từ mRNA được đưa vào chúng, thì có thể “coi RNA như một loại thuốc”. Một thành viên khác của phòng thí nghiệm Salk cũng đã ký các ghi chú để lưu lại hậu thế.
Cuối năm đó, các thí nghiệm của Malone cho thấy phôi ếch hấp thụ mRNA như vậy. Đây là lần đầu tiên có người sử dụng các giọt chất béo để dễ dàng truyền mRNA vào một cơ thể sống.
Những thí nghiệm đó là bước đệm để hướng tới hai loại vắc-xin quan trọng và có lợi nhất trong lịch sử: vắc-xin COVID-19 dựa trên mRNA được cung cấp cho hàng trăm triệu người trên thế giới.
Doanh thu toàn cầu của những sản phẩm vắc-xin này dự kiến sẽ đạt 50 tỷ đô la Mỹ chỉ riêng vào năm 2021.
Theo Nature.
Nhưng con đường dẫn đến thành công không trực tiếp. Trong nhiều năm sau các thí nghiệm của Malone, mà chính họ đã rút ra từ công trình của các nhà nghiên cứu khác, mRNA được coi là quá không ổn định và đắt tiền để được sử dụng như một loại thuốc hoặc vắc-xin.
Hàng chục phòng thí nghiệm học thuật và các công ty đã làm việc với ý tưởng này, vật lộn với việc tìm ra công thức phù hợp của chất béo và axit nucleic – những thành phần cơ bản của vắc xin mRNA.
Các mũi tiêm mRNA ngày nay có những cải tiến được phát minh nhiều năm sau thời gian Malone trong phòng thí nghiệm, bao gồm RNA được sửa đổi về mặt hóa học và các loại bong bóng chất béo khác nhau để đưa chúng vào tế bào.
Tuy nhiên, Malone, người tự gọi mình là “nhà phát minh ra vắc-xin mRNA”, cho rằng công việc của ông chưa được ghi nhận đầy đủ. “Tôi đã được viết ra khỏi lịch sử,” ông nói với Nature.
Bên trong vắc-xin mRNA
Vắc xin COVID-19 được làm từ mRNA sử dụng các hạt nano lipid – bong bóng chất béo để mang các phân tử vào tế bào. mRNA chứa mã để tế bào tạo ra protein ‘spike’ mà coronavirus SARS-CoV-2 sử dụng để xâm nhập vào tế bào.
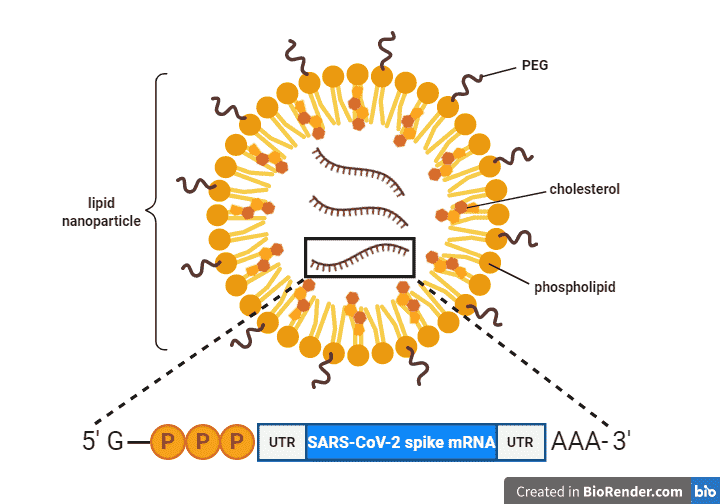
Dưới đây là những đổi mới chính trong thiết kế của các loại vắc-xin này:
- Các vắc-xin do Moderna và Pfizer-BioNTech sản xuất sử dụng mRNA đã được biến đổi về mặt hóa học để thay thế nucleotide uridine (U) bằng pseudouridine (Ψ). Sự thay đổi này được cho là để ngăn hệ thống miễn dịch phản ứng với mRNA được đưa vào.
- Để giúp cơ thể tăng cường phản ứng miễn dịch hiệu quả đối với các trường hợp nhiễm SARS-CoV-2 sau này, trình tự mRNA được điều chỉnh để ổn định protein spike theo hình dạng mà nó sử dụng khi kết hợp với tế bào người.
- Hạt nano béo xung quanh mRNA được tạo ra từ bốn loại phân tử lipid. Một trong số đó là ‘ion hóa’: trong vắc-xin, nhiều phân tử này mang điện tích dương và bám vào mRNA tích điện âm, nhưng chúng mất điện tích đó trong điều kiện kiềm hơn của máu, làm giảm độc tính trong cơ thể.
Cuộc tranh luận xem ai xứng đáng được công nhận vì đã đi tiên phong trong công nghệ đang nóng lên khi các giải thưởng bắt đầu được trao – và những đồn đoán ngày càng trở nên gay gắt hơn trước khi công bố giải Nobel vào tháng tới.
Nhưng các giải thưởng chính thức chỉ giới hạn cho một số nhà khoa học sẽ không công nhận nhiều người đóng góp cho sự phát triển y học của mRNA.
Trên thực tế, con đường tạo ra vắc-xin mRNA đã dựa trên công việc của hàng trăm nhà nghiên cứu trong hơn 30 năm.
Câu chuyện làm sáng tỏ cách mà nhiều khám phá khoa học trở thành phát kiến thay đổi cuộc sống: với nhiều thập kỷ đi vào ngõ cụt, bị từ chối và cuộc chiến tranh giành lợi nhuận tiềm năng, nhưng cũng là sự hào phóng, tò mò và kiên trì chống lại sự hoài nghi và hoài nghi.
Paul Krieg, một nhà sinh học phát triển tại Đại học Arizona ở Tucson, người đã đóng góp vào giữa những năm 1980, cho biết: “Đó là một chuỗi dài các bước,“ và bạn không bao giờ biết điều gì sẽ hữu ích ”.
Sự khởi đầu của mRNA
Các thí nghiệm của Malone không có gì đáng ngạc nhiên. Từ năm 1978, các nhà khoa học đã sử dụng cấu trúc màng chất béo được gọi là liposome để vận chuyển mRNA vào tế bào chuột và chuột để tạo ra sự biểu hiện protein.
Các liposome đóng gói và bảo vệ mRNA, sau đó kết hợp với màng tế bào để cung cấp vật liệu di truyền vào tế bào.
Bản thân những thí nghiệm này được xây dựng dựa trên nhiều năm làm việc với liposome và với mRNA; cả hai đều được phát hiện vào những năm 1960 (xem ‘Lịch sử của vắc xin mRNA’ tại đây).
Tuy nhiên, vào thời đó, rất ít nhà nghiên cứu nghĩ về mRNA như một sản phẩm y tế – đặc biệt là vì vẫn chưa có cách sản xuất vật liệu di truyền trong phòng thí nghiệm.
Thay vào đó, họ hy vọng sử dụng nó để hỏi dò các quá trình phân tử cơ bản. Hầu hết các nhà khoa học tái sử dụng mRNA từ máu thỏ, tế bào chuột nuôi cấy hoặc một số nguồn động vật khác.
Điều đó đã thay đổi vào năm 1984, khi Krieg và các thành viên khác của nhóm do nhà sinh học phát triển Douglas Melton dẫn đầu và các nhà sinh học phân tử Tom Maniatis và Michael Green tại Đại học Harvard ở Cambridge, Massachusetts, sử dụng một loại enzyme tổng hợp RNA (lấy từ vi-rút) và các công cụ khác.
Để tạo ra mRNA có hoạt tính sinh học trong phòng thí nghiệm – một phương pháp cốt lõi của nó vẫn được sử dụng cho đến ngày nay. Krieg sau đó đã tiêm mRNA do phòng thí nghiệm tạo ra vào trứng ếch và cho thấy rằng nó hoạt động giống như thật.
Cả Melton và Krieg đều nói rằng họ xem mRNA tổng hợp chủ yếu là một công cụ nghiên cứu để nghiên cứu chức năng và hoạt động của gen.
Năm 1987, sau khi Melton phát hiện ra rằng mRNA có thể được sử dụng cả để kích hoạt và ngăn chặn sản xuất protein, ông đã giúp thành lập một công ty có tên Oligogen (sau này đổi tên thành Gilead Sciences ở Foster City, California) để khám phá các cách sử dụng RNA tổng hợp để ngăn chặn biểu hiện của các gen mục tiêu – nhằm điều trị bệnh.
Bất kỳ ai trong phòng thí nghiệm của ông ấy, hay các cộng tác viên của họ đều không nghĩ đến vắc-xin.
Krieg nói: “RNA nói chung có tiếng là không ổn định không thể tin được. “Mọi thứ xung quanh RNA đều được che giấu cẩn thận.”
Điều đó có thể giải thích tại sao văn phòng phát triển công nghệ của Harvard đã chọn không cấp bằng sáng chế cho phương pháp tổng hợp RNA của nhóm.
Thay vào đó, các nhà nghiên cứu Harvard chỉ cần đưa thuốc thử của họ cho Promega Corporation, một công ty cung cấp vật tư phòng thí nghiệm ở Madison, Wisconsin, nơi cung cấp các công cụ tổng hợp RNA cho các nhà nghiên cứu.
Họ nhận được tiền bản quyền khiêm tốn và đổi lại là một hộp rượu Champagne Veuve Clicquot.
Tranh chấp bằng sáng chế
Nhiều năm sau, Malone làm theo chiến thuật của nhóm Harvard để tổng hợp mRNA cho các thí nghiệm của ông.
Nhưng ông đã bổ sung một loại liposome mới, một loại mang điện tích dương, giúp tăng cường khả năng tương tác của vật liệu với xương sống mang điện tích âm của mRNA.
Những liposome này được phát triển bởi Philip Felgner, một nhà hóa sinh học, hiện là lãnh đạo Trung tâm Nghiên cứu và Phát triển Vắc-xin tại Đại học California, Irvine.
Mặc dù đã thành công khi sử dụng liposome để cung cấp mRNA vào tế bào người và phôi ếch, Malone chưa bao giờ lấy được bằng tiến sĩ.
Ông ấy đã bất hòa với người giám sát của mình, nhà nghiên cứu liệu pháp gen Salk, Inder Verma và vào năm 1989, bỏ dở việc học sau đại học sớm để làm việc cho Felgner tại Vical, một công ty mới thành lập gần đây ở San Diego, California.
Tại đó, họ và các cộng tác viên tại Đại học Wisconsin-Madison đã chỉ ra rằng phức hợp lipid-mRNA có thể thúc đẩy sản xuất protein ở chuột.
Sau đó, mọi thứ trở nên lộn xộn. Cả Vical (với Đại học Wisconsin) và Salk đều bắt đầu nộp đơn xin cấp bằng sáng chế vào tháng 3 năm 1989.
Nhưng Salk sớm từ bỏ yêu cầu cấp bằng sáng chế của ông, và vào năm 1990, Verma gia nhập ban cố vấn của Vical.
Malone cho rằng Verma và Vical đã thực hiện một thỏa thuận phòng the để tài sản trí tuệ liên quan được chuyển cho Vical.
Malone được liệt vào danh sách một nhà phát minh trong số nhiều nhà phát minh, nhưng ông ta không còn thu lợi cá nhân từ các hợp đồng cấp phép tiếp theo, như ông ta sẽ có từ bất kỳ bằng sáng chế nào do Salk cấp.
Malone rời Vical vào tháng 8 năm 1989, với lý do bất đồng với Felgner về “đánh giá khoa học” và “công nhận cho những đóng góp trí tuệ của tôi”.
Ông ấy đã hoàn thành trường y khoa và thực hiện một năm đào tạo lâm sàng trước khi làm việc trong học viện, nơi ông ấy cố gắng tiếp tục nghiên cứu về vắc-xin mRNA nhưng phải vật lộn để đảm bảo tài trợ.
Ví dụ, vào năm 1996, ông đã không thành công khi nộp đơn xin tiền cho một cơ quan nghiên cứu của bang California để phát triển một loại vắc-xin mRNA để chống lại nhiễm trùng coronavirus theo mùa.
Theo Nature.
Thay vào đó, Malone tập trung vào vắc-xin DNA và công nghệ phân phối.
Năm 2001, ông chuyển sang công việc thương mại và tư vấn. Và trong vài tháng qua, ông đã bắt đầu công khai tính an toàn của vắc-xin mRNA mà nghiên cứu của ông đã giúp kích hoạt.
Ví dụ, Malone nói rằng các protein được tạo ra bởi vắc-xin có thể làm hỏng các tế bào của cơ thể và rủi ro của việc tiêm chủng lớn hơn lợi ích đối với trẻ em và thanh niên – tuyên bố rằng các nhà khoa học và quan chức y tế khác đã nhiều lần bác bỏ.
Thách thức sản xuất
Năm 1991, Vical tham gia hợp tác nghiên cứu trị giá hàng triệu đô la và thỏa thuận cấp phép với công ty Merck của Mỹ, một trong những nhà phát triển vắc-xin lớn nhất thế giới.
Các nhà khoa học Merck đã đánh giá công nghệ mRNA trên chuột với mục đích tạo ra vắc-xin cúm, nhưng sau đó đã từ bỏ cách tiếp cận đó.
Jeffrey Ulmer, một cựu nhà khoa học của Merck, người hiện đang tư vấn cho các công ty về các vấn đề nghiên cứu vắc-xin cho biết: “Chi phí và tính khả thi của việc sản xuất đã khiến chúng tôi tạm dừng.
Các nhà nghiên cứu tại một công ty công nghệ sinh học nhỏ ở Strasbourg, Pháp, có tên là Transgène, cũng cảm thấy như vậy.
Ở đó, vào năm 1993, một nhóm do Pierre Meulien dẫn đầu, làm việc với các đối tác công nghiệp và học thuật, là người đầu tiên chỉ ra rằng mRNA trong liposome có thể tạo ra một phản ứng miễn dịch kháng vi-rút cụ thể ở chuột.
Một tiến bộ thú vị khác đã đến vào năm 1992, khi các nhà khoa học tại Viện nghiên cứu Scripps ở La Jolla sử dụng mRNA để thay thế một loại protein bị thiếu hụt ở chuột, nhằm điều trị chứng rối loạn chuyển hóa. Nhưng phải mất gần hai thập kỷ trước khi các phòng thí nghiệm độc lập báo cáo thành công tương tự.
Theo Nature.
Các nhà nghiên cứu Transgène đã cấp bằng sáng chế cho phát minh của họ và tiếp tục nghiên cứu vắc-xin mRNA.
Nhưng Meulien, hiện là người đứng đầu Sáng kiến Thuốc cải tiến, một doanh nghiệp tư nhân có trụ sở tại Brussels, ước tính rằng ông ấy cần ít nhất 100 triệu euro (119 triệu đô la Mỹ) để tối ưu hóa nền tảng – và ông ấy không định hỏi ông chủ cho nhiều như vậy cho một mạo hiểm “khó khăn, rủi ro cao” như vậy, ông nói.
Bằng sáng chế hết hiệu lực sau khi công ty mẹ của Transgène quyết định ngừng trả các khoản phí cần thiết để duy trì hoạt động.
Nhóm của Meulien, giống như nhóm Merck, thay vào đó tập trung vào vắc-xin DNA và các hệ thống phân phối dựa trên véc-tơ khác.
Nền tảng DNA cuối cùng đã mang lại một số vắc-xin được cấp phép cho các ứng dụng thú y – chẳng hạn như giúp ngăn ngừa nhiễm trùng trong các trang trại cá.
Và mới tháng trước, các cơ quan quản lý ở Ấn Độ đã cấp phép khẩn cấp cho vắc-xin DNA đầu tiên trên thế giới dùng cho con người, để giúp ngăn chặn COVID-19.
Nhưng vì những lý do chưa được hiểu rõ ràng, vắc-xin DNA đã chậm tìm thấy thành công ở người.
Tuy nhiên, nỗ lực phối hợp của ngành xung quanh công nghệ DNA cũng mang lại lợi ích cho vắc-xin RNA, Ulmer lập luận.
Từ việc cân nhắc sản xuất và kinh nghiệm quy định đến thiết kế trình tự và hiểu biết phân tử, “nhiều điều chúng tôi học được từ DNA có thể được áp dụng trực tiếp cho RNA”, ông nói. “Nó cung cấp nền tảng cho sự thành công của RNA.”
Đấu tranh liên tục
Trong những năm 1990 và trong hầu hết những năm 2000, gần như mọi công ty vắc-xin cân nhắc làm việc trên mRNA đều chọn đầu tư nguồn lực của mình vào nơi khác. Sự hiểu biết thông thường cho rằng mRNA quá dễ bị suy thoái và việc sản xuất nó quá đắt.
Peter Liljeström, nhà vi-rút học tại Viện Karolinska ở Stockholm, cho biết: “Đó là một cuộc đấu tranh liên tục,” cho biết 30 năm trước, người đã đi tiên phong trong một loại vắc-xin RNA ‘tự khuếch đại’.
Matt Winkler, người thành lập một trong những công ty cung cấp vật tư phòng thí nghiệm tập trung vào RNA đầu tiên, Ambion, ở Austin, Texas, nói: “RNA rất khó làm việc vào năm 1989.“ Nếu bạn hỏi lại tôi [thì] liệu bạn có thể tiêm RNA vào ai đó để làm vắc-xin, tôi sẽ cười vào mặt bạn.”
Ý tưởng vắc-xin mRNA đã được tiếp nhận thuận lợi hơn trong giới ung thư học, mặc dù như một tác nhân điều trị, hơn là để ngăn ngừa bệnh tật.
Bắt đầu với công việc của nhà trị liệu gen David Curiel, một số nhà khoa học hàn lâm và các công ty mới thành lập đã tìm hiểu xem liệu mRNA có thể được sử dụng để chống lại bệnh ung thư hay không.
Nếu các protein mã hóa mRNA được biểu hiện bởi các tế bào ung thư, thì việc tiêm nó vào cơ thể có thể huấn luyện hệ thống miễn dịch để tấn công các tế bào đó.
Curiel, hiện đang làm việc tại Trường Y Đại học Washington ở St Louis, Missouri, đã có một số thành công trên chuột. Nhưng khi ông ấy tiếp cận Ambion về các cơ hội thương mại hóa, ông ấy nói, công ty đã nói với ông ấy: “Chúng tôi không thấy bất kỳ tiềm năng kinh tế nào trong công nghệ này”.
Một nhà miễn dịch học ung thư khác đã thành công hơn, dẫn đến việc thành lập công ty điều trị mRNA đầu tiên vào năm 1997.
Eli Gilboa đề xuất lấy các tế bào miễn dịch từ máu và dụ chúng sử dụng mRNA tổng hợp mã hóa các protein khối u. Sau đó, các tế bào sẽ được tiêm trở lại cơ thể, nơi chúng có thể điều khiển hệ thống miễn dịch tấn công các khối u ẩn nấp.
Gilboa và các đồng nghiệp của ông tại Trung tâm Y tế Đại học Duke ở Durham, Bắc Carolina, đã chứng minh điều này trên chuột.
Vào cuối những năm 1990, các cộng tác viên học thuật đã khởi động các thử nghiệm trên người, và sản phẩm thương mại của Gilboa, Merix Bioscience (sau đó được đổi tên thành Argos Therapeutics và bây giờ được gọi là CoImmune), ngay sau đó là các nghiên cứu lâm sàng của riêng ông.
Cách tiếp cận này có vẻ hứa hẹn cho đến một vài năm trước, khi một loại vắc-xin ứng cử viên giai đoạn cuối thất bại trong một cuộc thử nghiệm lớn; nó bây giờ phần lớn đã không còn hợp thời nữa.
Nhưng việc làm của Gilboa có một hệ quả quan trọng. Nó đã truyền cảm hứng cho những người sáng lập của các công ty Đức CureVac và BioNTech – hai trong số các công ty mRNA lớn nhất hiện nay – bắt đầu làm việc trên mRNA.
Cả Ingmar Hoerr, tại CureVac và Uğur Şahin, tại BioNTech, nói với Nature rằng, sau khi biết những gì Gilboa đã làm, họ muốn làm điều tương tự, nhưng bằng cách đưa mRNA trực tiếp vào cơ thể.
Gilboa, hiện đang làm việc tại Trường Y khoa Đại học Miami Miller ở Florida, cho biết: “Có một hiệu ứng quả cầu tuyết.”
Tăng tốc khởi nghiệp
Hoerr là người đầu tiên đạt được thành công. Khi ở Đại học Tübingen ở Đức, ông đã báo cáo vào năm 2000 rằng tiêm trực tiếp có thể tạo ra phản ứng miễn dịch ở chuột.
Ông ấy đã tạo ra CureVac (cũng có trụ sở tại Tübingen) vào năm đó. Nhưng có vẻ ít nhà khoa học hoặc nhà đầu tư quan tâm.
Tại một hội nghị, nơi Hoerr trình bày dữ liệu ban đầu về chuột, ông ấy nói, “có một người đoạt giải Nobel đứng ở hàng đầu tiên và nói,“ Đây hoàn toàn là những gì bạn đang nói với chúng tôi ở đây – hoàn toàn tồi tệ ”.” (Hoerr từ chối nêu tên người đoạt giải Nobel.)
Cuối cùng, tiền cũng đổ về. Và trong vài năm, thử nghiệm trên người đã bắt đầu. Giám đốc khoa học của công ty vào thời điểm đó, Steve Pascolo, là đối tượng nghiên cứu đầu tiên: ông ta đã tự tiêm mRNA cho mình và vẫn có những vết sẹo trắng to bằng đầu người ở chân do một bác sĩ da liễu lấy mẫu sinh thiết đục lỗ để phân tích.
Một thử nghiệm chính thức hơn, liên quan đến mRNA đặc hiệu cho khối u cho những người bị ung thư da, đã bắt đầu ngay sau đó.
Şahin và vợ nhà miễn dịch học của ông, Özlem Türeci, cũng bắt đầu nghiên cứu mRNA vào cuối những năm 1990, nhưng đợi lâu hơn Hoerr để thành lập công ty.
Họ nghiên cứu công nghệ trong nhiều năm, làm việc tại Đại học Johannes Gutenberg Mainz ở Đức, kiếm bằng sáng chế, giấy tờ và tài trợ nghiên cứu, trước khi đưa ra một kế hoạch thương mại cho các nhà đầu tư tỷ phú vào năm 2007.
“Nếu nó hoạt động, nó sẽ là bước đột phá, ”Şahin nói. Ông ấy đã nhận được 150 triệu euro tiền tài trợ.
Cùng năm đó, một công ty khởi nghiệp mRNA non trẻ có tên là RNARx đã nhận được một khoản tiền khiêm tốn hơn: 97.396 USD tiền tài trợ dành cho doanh nghiệp nhỏ từ chính phủ Hoa Kỳ.
Những người sáng lập công ty, nhà hóa sinh Katalin Karikó và nhà miễn dịch học Drew Weissman, cả hai khi đó tại Đại học Pennsylvania (UPenn) ở Philadelphia, đã đưa ra một phát hiện quan trọng mà ngày nay người ta cho rằng: việc thay đổi một phần của mã mRNA giúp mRNA tổng hợp vượt qua khả năng bảo vệ miễn dịch bẩm sinh của tế bào.
Thông tin chi tiết cơ bản
Karikó đã làm việc trong phòng thí nghiệm trong suốt những năm 1990 với mục tiêu biến mRNA thành một nền tảng thuốc, mặc dù các cơ quan tài trợ liên tục từ chối các đơn xin tài trợ của bà.
Năm 1995, sau nhiều lần bị từ chối, bà được lựa chọn rời bỏ UPenn hoặc chấp nhận cách chức và cắt lương.
Bà đã chọn ở lại và tiếp tục theo đuổi kiên trì của mình, cải tiến các giao thức của Malone, và quản lý để khiến các tế bào sản sinh ra một loại protein lớn và phức tạp có liên quan đến điều trị.
Năm 1997, bà bắt đầu làm việc với Weissman, người mới bắt đầu một phòng thí nghiệm tại UPenn.
Họ cùng nhau lên kế hoạch phát triển một loại vắc-xin dựa trên mRNA cho HIV / AIDS. Nhưng mRNA của Karikó gây ra phản ứng viêm lớn khi chúng được tiêm vào chuột.
Bà và Weissman đã sớm tìm ra lý do tại sao: mRNA tổng hợp đã kích thích chuỗi cảm biến miễn dịch được gọi là các thụ thể giống như Toll, hoạt động như những phản ứng đầu tiên đối với các tín hiệu nguy hiểm từ mầm bệnh.
Năm 2005, cặp đôi báo cáo rằng việc sắp xếp lại các liên kết hóa học trên một trong các nucleotide của mRNA, uridine, để tạo ra một chất tương tự gọi là pseudouridine, dường như ngăn cơ thể xác định mRNA là kẻ thù.
Rất ít nhà khoa học vào thời điểm đó đã công nhận giá trị chữa bệnh của những nucleotide biến đổi này. Nhưng giới khoa học đã sớm đánh thức tiềm năng của chúng.
Vào tháng 9 năm 2010, một nhóm nghiên cứu do Derrick Rossi, một nhà sinh học tế bào gốc tại Bệnh viện Nhi Boston ở Massachusetts, đã mô tả cách mRNA đã sửa đổi có thể được sử dụng để biến đổi tế bào da, trước tiên thành tế bào gốc giống phôi thai và sau đó thành mô cơ co lại.
Phát hiện đã tạo ra một sự chú ý lớn. Rossi được tạp chí Time bình chọn là một trong những ‘người quan trọng’ của năm 2010. Ông ấy đồng sáng lập một công ty khởi nghiệp, Moderna ở Cambridge.
Moderna đã cố gắng cấp bằng sáng chế cho mRNA sửa đổi mà UPenn đã nộp vào năm 2006 cho phát minh của Karikó và Weissman. Nhưng đã quá trễ rồi.
Sau khi không đạt được thỏa thuận cấp phép với RNARx, UPenn đã chọn thanh toán nhanh chóng.
Vào tháng 2 năm 2010, nó đã cấp độc quyền bằng sáng chế cho một nhà cung cấp thuốc thử nhỏ trong phòng thí nghiệm ở Madison. Bây giờ được gọi là Cellscript, công ty đã trả 300.000 đô la trong thương vụ này.
Nó sẽ tiếp tục thu về hàng trăm triệu đô la phí cấp phép phụ từ Moderna và BioNTech, những người sản xuất vắc-xin mRNA đầu tiên cho COVID-19. Cả hai sản phẩm đều chứa mRNA đã được sửa đổi.
Trong khi đó, RNARx đã sử dụng hết 800.000 USD tiền tài trợ dành cho doanh nghiệp nhỏ và ngừng hoạt động vào năm 2013, vào khoảng thời gian Karikó gia nhập BioNTech (giữ lại một cuộc hẹn bổ sung tại UPenn).
Cuộc tranh luận về pseudouridine
Các nhà nghiên cứu vẫn tranh cãi về việc liệu khám phá của Karikó và Weissman có cần thiết cho việc tiêm vắc-xin mRNA thành công hay không.
Moderna luôn sử dụng mRNA đã được sửa đổi – tên của nó là từ ghép của hai từ đó. Nhưng một số người khác trong ngành thì không.
Các nhà nghiên cứu tại bộ phận trị liệu di truyền-con người của công ty dược phẩm Shire ở Lexington, Massachusetts, lý giải rằng mRNA không bị biến đổi có thể tạo ra một sản phẩm có hiệu quả tương đương nếu các cấu trúc ‘nắp’ phù hợp được thêm vào và loại bỏ tất cả các tạp chất.
Michael Heartlein, người dẫn đầu nỗ lực nghiên cứu của Shire và tiếp tục cải tiến công nghệ tại Translate Bio ở Cambridge, cho biết: “Nó phụ thuộc vào chất lượng của RNA,” đây cũng là nơi Shire sau đó đã bán danh mục mRNA của mình. (Shire hiện là một phần của công ty Nhật Bản Takeda.)
Mặc dù Translate có một số dữ liệu về con người cho thấy mRNA của nó không gây ra phản ứng miễn dịch liên quan, nhưng nền tảng của nó vẫn được chứng minh trên lâm sàng: ứng cử viên vắc-xin COVID-19 của nó vẫn đang trong quá trình thử nghiệm ban đầu trên người.
Nhưng gã khổng lồ về thuốc của Pháp Sanofi đã bị thuyết phục về lời hứa của công nghệ: vào tháng 8 năm 2021, họ công bố kế hoạch mua lại Translate với giá 3,2 tỷ USD. (Heartlein rời năm ngoái để thành lập một công ty khác ở Waltham, Massachusetts, có tên là Maritime Therapeutics.)
Trong khi đó, CureVac có chiến lược giảm thiểu miễn dịch của riêng họ, liên quan đến việc thay đổi trình tự di truyền của mRNA để giảm thiểu lượng uridine trong vắc-xin của nó.
Hai mươi năm làm việc theo cách tiếp cận đó dường như đã mang lại kết quả, với những thử nghiệm ban đầu đối với vắc-xin thử nghiệm bệnh dại và COVID-19 đều chứng tỏ thành công.
Nhưng vào tháng 6, dữ liệu từ một thử nghiệm giai đoạn sau cho thấy ứng cử viên vắc-xin coronavirus của CureVac có khả năng bảo vệ kém hơn nhiều so với của Moderna hoặc BioNTech’s.
Dựa trên những kết quả đó, một số chuyên gia mRNA hiện coi pseudouridine là một thành phần thiết yếu của công nghệ – và do đó, họ nói, khám phá của Karikó và Weissman là một trong những đóng góp quan trọng đáng được ghi nhận và nhận giải thưởng.
Jake Becraft, đồng sáng lập và giám đốc điều hành của Strand Therapeutics, một công ty sinh học tổng hợp có trụ sở tại Cambridge, đang nghiên cứu về phương pháp trị liệu dựa trên mRNA cho biết: “Người chiến thắng thực sự ở đây là RNA đã được sửa đổi.
Không phải ai cũng chắc chắn như vậy. “Có nhiều yếu tố có thể ảnh hưởng đến sự an toàn và hiệu quả của vắc-xin mRNA, biến đổi hóa học của mRNA chỉ là một trong số đó” theo Bo Ying, giám đốc điều hành của Suzhou Abogen Biosciences, một công ty Trung Quốc sản xuất vắc-xin mRNA cho COVID-19 bây giờ đang trong giai đoạn cuối thử nghiệm lâm sàng. (Được gọi là ARCoV, sản phẩm sử dụng mRNA chưa được sửa đổi.)
Đột phá về chất béo
Đối với công nghệ linchpin, nhiều chuyên gia nhấn mạnh một sự đổi mới khác rất quan trọng đối với vắc-xin mRNA – một cải tiến không liên quan gì đến mRNA.
Đó là các bong bóng chất béo nhỏ được gọi là hạt nano lipid, hoặc LNP, bảo vệ mRNA và đưa nó vào tế bào.
Công nghệ này đến từ phòng thí nghiệm của Pieter Cullis, một nhà hóa sinh tại Đại học British Columbia ở Vancouver, Canada, và một số công ty do ông sáng lập hoặc lãnh đạo.
Bắt đầu từ cuối những năm 1990, họ đã đi tiên phong trong việc cung cấp các chuỗi axit nucleic giúp ngăn chặn hoạt động của gen.
Một phương pháp điều trị như vậy, patisiran, hiện đã được chấp thuận cho một căn bệnh di truyền hiếm gặp.
Sau khi liệu pháp làm gene-silencing đó bắt đầu có triển vọng trong các thử nghiệm lâm sàng, vào năm 2012, hai trong số các công ty của Cullis đã xoay trục để khám phá các cơ hội cho hệ thống phân phối LNP trong các loại thuốc dựa trên mRNA.
Ví dụ, Acuitas Therapeutics ở Vancouver, do giám đốc điều hành Thomas Madden dẫn đầu, đã tạo dựng quan hệ đối tác với nhóm của Weissman tại UPenn và với một số công ty mRNA để thử nghiệm các công thức mRNA-LNP khác nhau.
Một trong những điều này hiện có thể được tìm thấy trong vắc-xin COVID-19 của BioNTech và CureVac. Cách pha chế LNP của Moderna không khác nhiều.
Các hạt nano có một hỗn hợp của bốn phân tử chất béo: ba đóng góp vào cấu trúc và sự ổn định; loại thứ tư, được gọi là lipid có thể ion hóa, là chìa khóa thành công của LNP.
Chất này được tích điện dương trong điều kiện phòng thí nghiệm, mang lại những ưu điểm tương tự như liposome mà Felgner đã phát triển và Malone đã thử nghiệm vào cuối những năm 1980.
Nhưng các chất béo có thể ion hóa do Cullis và các đối tác thương mại của ông cải tiến sẽ chuyển đổi thành điện tích trung tính trong các điều kiện sinh lý như trong máu, giúp hạn chế tác động độc hại lên cơ thể.
Hơn nữa, loại cocktail 4 lipid cho phép sản phẩm được lưu trữ lâu hơn trên kệ thuốc và duy trì sự ổn định bên trong cơ thể, Ian MacLachlan, cựu giám đốc điều hành tại một số công ty liên kết với Cullis cho biết. “Đó là toàn bộ bộ dụng cụ và caboodle dẫn đến dược lý mà chúng tôi có bây giờ,” ông nói.
Vào giữa những năm 2000, một phương pháp mới để trộn và sản xuất các hạt nano này đã được đưa ra.
Nó liên quan đến việc sử dụng thiết bị ‘đầu nối T’, kết hợp chất béo (hòa tan trong rượu) với axit nucleic (hòa tan trong dung dịch đệm axit). Khi các luồng của hai dung dịch kết hợp với nhau, các thành phần tự phát hình thành các LNPs dày đặc.
Nó được chứng minh là một kỹ thuật đáng tin cậy hơn các cách khác để sản xuất thuốc dựa trên mRNA.
Andrew Geall, hiện là giám đốc phát triển của Replicate Bioscience ở San Diego, cho biết một khi tất cả các mảnh ghép lại với nhau, “nó giống như một làn khói thánh, cuối cùng chúng ta đã có một quy trình mà chúng ta có thể mở rộng quy mô”.
Geall đã dẫn đầu nhóm đầu tiên kết hợp LNP với vắc-xin RNA, tại trung tâm Novartis của Hoa Kỳ ở Cambridge vào năm 2012.
Mỗi công ty mRNA hiện sử dụng một số biến thể của nền tảng phân phối và hệ thống sản xuất LNP này – mặc dù ai sở hữu bằng sáng chế liên quan vẫn là đối tượng pháp lý tranh chấp.
Moderna, chẳng hạn, bị khóa trong cuộc chiến với một doanh nghiệp liên kết với Cullis – Arbutus Biopharma ở Vancouver – về người nắm giữ quyền đối với công nghệ LNP được tìm thấy trong COVID-19 của Moderna.
Một ngành công nghiệp được sinh ra
Vào cuối những năm 2000, một số công ty dược phẩm lớn đã tham gia vào lĩnh vực mRNA.
Ví dụ, vào năm 2008, cả Novartis và Shire đều thành lập đơn vị nghiên cứu mRNA – đơn vị trước (do Geall lãnh đạo) tập trung vào vắc-xin, đơn vị sau (do Heartlein lãnh đạo) về trị liệu.
BioNTech ra mắt vào năm đó và các công ty khởi nghiệp khác nhanh chóng bước vào cuộc cạnh tranh, được hỗ trợ bởi quyết định năm 2012 của Cơ quan Dự án Nghiên cứu Tiên tiến Quốc phòng Hoa Kỳ về việc bắt đầu tài trợ cho các nhà nghiên cứu trong ngành để nghiên cứu vắc-xin và thuốc RNA.
Moderna là một trong những công ty đã xây dựng dựa trên công việc này và đến năm 2015, nó đã huy động được hơn 1 tỷ đô la với lời hứa khai thác mRNA để cảm ứng các tế bào trong cơ thể tự sản xuất thuốc – do đó sửa chữa các bệnh do protein bị thiếu hoặc bị lỗi gây ra.
Khi kế hoạch đó bị thất bại, Moderna, do giám đốc điều hành Stéphane Bancel dẫn đầu, đã chọn ưu tiên cho một mục tiêu ít tham vọng hơn: chế tạo vắc-xin.
Điều đó ban đầu khiến nhiều nhà đầu tư và người xem thất vọng vì nền tảng vắc-xin dường như ít biến đổi và sinh lợi hơn.
Đến đầu năm 2020, Moderna đã nâng cấp chín ứng cử viên vắc-xin mRNA cho các bệnh truyền nhiễm vào người để thử nghiệm. Không cái nào là một thành công của slam-dunk. Chỉ một cái đã tiến tới thử nghiệm giai đoạn lớn hơn.
Nhưng khi COVID-19 xuất hiện, Moderna đã nhanh chóng đi ra ngoài dấu ấn, tạo ra một loại vắc-xin nguyên mẫu trong vòng vài ngày kể từ khi trình tự bộ gen của vi-rút có sẵn trên mạng.
Sau đó, công ty đã hợp tác với Viện Dị ứng và Bệnh truyền nhiễm Quốc gia Hoa Kỳ (NIAID) để tiến hành các nghiên cứu trên chuột và khởi động các thử nghiệm trên người, tất cả chỉ trong vòng chưa đầy mười tuần.
BioNTech cũng vậy, đã thực hiện một cách tiếp cận toàn diện.
Vào tháng 3 năm 2020, họ hợp tác với công ty dược phẩm Pfizer có trụ sở tại New York, và các thử nghiệm lâm sàng sau đó đã diễn ra với tốc độ kỷ lục, từ thử nghiệm đầu tiên trên người đến phê duyệt khẩn cấp trong vòng chưa đầy tám tháng.
Cả hai loại vắc-xin được ủy quyền đều sử dụng công thức mRNA đã được sửa đổi trong LNPs.
Cả hai cũng chứa các trình tự mã hóa một dạng của protein đột biến SARS-CoV-2 có hình dạng phù hợp hơn để tạo ra khả năng miễn dịch bảo vệ.
Nhiều chuyên gia nói rằng việc tinh chỉnh protein, do nhà tiêm chủng Barney Graham của NIAID và nhà sinh học cấu trúc Jason McLellan tại Đại học Texas ở Austin và Andrew Ward tại Scripps nghĩ ra, cũng là một đóng góp xứng đáng, mặc dù là một đóng góp dành riêng cho vắc-xin coronavirus, không phải tiêm chủng mRNA như một nền tảng chung.
Một số ý kiến phản đối trong các cuộc thảo luận về tín dụng cho các khám phá mRNA liên quan đến việc ai nắm giữ các bằng sáng chế sinh lợi.
Nhưng phần lớn tài sản trí tuệ cơ bản bắt nguồn từ các tuyên bố được đưa ra vào năm 1989 bởi Felgner, Malone và các đồng nghiệp của họ tại Vical (và vào năm 1990 bởi Liljeström).
Chúng chỉ có thời hạn 17 năm kể từ ngày phát hành và do đó hiện đã nằm trong phạm vi công cộng.
Ngay cả bằng sáng chế của Karikó – Weissman, được cấp phép cho Cellscript và được nộp vào năm 2006, sẽ hết hạn trong năm năm tới.
Những người trong ngành cho biết điều này có nghĩa là sẽ rất khó để cấp bằng sáng chế cho các tuyên bố rộng rãi về việc cung cấp mRNA trong các hạt nano lipid, mặc dù các công ty có thể cấp bằng sáng chế một cách hợp lý cho các trình tự cụ thể của mRNA – một dạng protein đột biến – hoặc các công thức lipid độc quyền.
Các hãng đang cố gắng. Moderna, người chơi thống trị trong lĩnh vực vắc-xin mRNA, có các mũi tiêm thử nghiệm trong thử nghiệm lâm sàng đối với bệnh cúm, cytomegalovirus và một loạt các bệnh truyền nhiễm khác, đã nhận được hai bằng sáng chế vào năm ngoái về việc sử dụng rộng rãi mRNA để sản xuất các protein tiết ra.
Nhưng nhiều người trong ngành nói với Nature rằng họ nghĩ rằng những thứ này có thể thách thức được.
Eric Marcusson, giám đốc khoa học của Providence Therapeutics, một công ty vắc-xin mRNA ở Calgary, Canada cho biết: “Chúng tôi không cảm thấy có nhiều thứ có thể được cấp bằng sáng chế và chắc chắn là không thể thực thi.”
Cuộc tranh luận Nobel
Đối với người xứng đáng nhận giải Nobel, những cái tên thường được nhắc đến trong cuộc trò chuyện là Karikó và Weissman.
Cả hai đã giành được một số giải thưởng, bao gồm một trong những Giải thưởng Đột phá (trị giá 3 triệu đô la, giải thưởng sinh lợi nhất trong khoa học) và Giải thưởng Công chúa Asturias danh giá của Tây Ban Nha về Nghiên cứu Khoa học và Kỹ thuật.
Cùng được công nhận trong giải thưởng Asturias còn có Felgner, Şahin, Türeci và Rossi, cùng với Sarah Gilbert, nhà tiêm chủng đứng sau vắc-xin COVID-19 do Đại học Oxford, Vương quốc Anh phát triển và công ty dược phẩm AstraZeneca, sử dụng véc-tơ vi-rút thay vì mARN.
Giải thưởng duy nhất gần đây của Cullis là giải thưởng của người sáng lập trị giá 5.000 đô la từ Hiệp hội Phát hành có Kiểm soát, một tổ chức chuyên nghiệp của các nhà khoa học nghiên cứu các loại thuốc giải phóng thời gian.
Theo Nature.
Một số người cũng cho rằng Karikó nên được ghi nhận nhiều vì những đóng góp của bà ấy cho cộng đồng nghiên cứu mRNA nói chung cũng như những khám phá của bà ấy trong phòng thí nghiệm.
Anna Blakney, một nhà kỹ thuật sinh học RNA tại Đại học British Columbia cho biết: “Bà ấy không chỉ là một nhà khoa học đáng kinh ngạc, mà còn là một động lực trong lĩnh vực này.”
Blakney ghi công cho Karikó khi cho bà ấy một vị trí phát biểu tại một hội nghị lớn hai năm trước, khi bà ấy vẫn còn ở vị trí postdoc cấp dưới (và trước khi Blakney đồng sáng lập VaxEquity, một công ty vắc-xin ở Cambridge, Vương quốc Anh, tập trung vào việc tự khuếch đại – Công nghệ RNA).
Karikó “đang tích cực cố gắng nâng người khác lên trong thời điểm mà bà ấy không được công nhận trong toàn bộ sự nghiệp của mình”.
Mặc dù một số người tham gia vào sự phát triển của mRNA, bao gồm cả Malone, nghĩ rằng họ xứng đáng được công nhận nhiều hơn, những người khác sẵn sàng chia sẻ ánh đèn sân khấu hơn. “Bạn thực sự không thể yêu cầu tín dụng,” Cullis nói.
Ví dụ, khi nói đến hệ thống phân phối lipid của ông ấy, “chúng ta đang nói đến hàng trăm, có lẽ là hàng nghìn người đã làm việc cùng nhau để tạo ra các hệ thống LNP này để chúng thực sự sẵn sàng cho thời gian quan trọng”.
Karikó nói: “Mọi người đều chỉ dần dần thêm một thứ gì đó – kể cả tôi.
Nhìn lại, nhiều người nói rằng họ chỉ vui mừng vì vắc-xin mRNA đang tạo ra sự khác biệt cho nhân loại và rằng chúng có thể đã đóng góp có giá trị trong suốt chặng đường.
Felgner nói: “Thật là hồi hộp cho tôi khi thấy điều này. “Tất cả những điều mà chúng tôi nghĩ sẽ xảy ra hồi đó – nó đang diễn ra ngay bây giờ.”
Bài viết đến đây là hết rồi. Hi vọng sẽ giúp ích cho các bạn phần nào trong tương lai. Lần sau nếu có ai hỏi về chủ đề này thì hãy nhớ về hóa học đằng sau chúng nhé
Tham khảo Nature.
